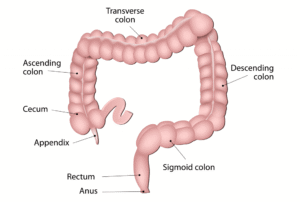
Рак на дебелото черво
Колоректалният рак (CRC), известен също като рак на червата, рак на дебелото черво или рак на ректума, представлява развитие на злокачествен тумор от дебелото черво или ректума (части от дебелото черво). Признаците и симптомите могат да включват кръв в изпражненията, промяна в изхожданията, загуба на тегло, коремна болка и умора. Повечето случаи на колоректален рак се дължат на фактори, свързани с начина на живот, и на генетични заболявания. Рисковите фактори включват хранителен режим, затлъстяване, тютюнопушене и липса на физическа активност. Хранителни фактори, които увеличават риска, са червеното месо, преработеното месо и алкохолът. Друг рисков фактор е възпалителното заболяване на червата, което включва болестта на Крон и улцерозния колит. Някои наследствени генетични заболявания, които могат да причинят колоректален рак, са фамилната аденоматозна полипоза и синдрома на Lynch, но те представляват по-малко от 5% от случаите. Обикновено ракът започва като доброкачествен тумор, често под формата на полип, който с времето се превръща в злокачествен.
Колоректалният рак може да бъде диагностициран чрез вземане на проба от дебелото черво по време на сигмоидоскопия или колоноскопия. След това се прави медицинско образно изследване, за да се определи дали болестта се е разпространила. Скринингът е ефективен за предотвратяване и намаляване на смъртността от колоректален рак. Препоръчва се скрининг с един от няколко метода за хора на възраст от 45 до 75 години. Преди се препоръчваше скринингът да започва на 50 години, но възрастта бе намалена на 45 поради увеличаващия се брой случаи. По време на колоноскопия могат да бъдат премахнати малки полипи, ако бъдат открити. Ако се открие голям полип или тумор, може да се направи биопсия, за да се провери дали е злокачествен. Аспиринът и други нестероидни противовъзпалителни лекарства намаляват риска от болка при премахване на полипи, но не се препоръчва общата им употреба за тази цел поради странични ефекти.
Лечението на колоректалния рак може да включва комбинация от хирургия, лъчетерапия, химиотерапия и таргетна терапия. Раковите заболявания, ограничени в стената на дебелото черво, могат да бъдат излекувани с операция, докато разпространеният рак обикновено не може да бъде излекуван и лечението е насочено към подобряване на качеството на живот и симптомите. Петгодишната преживяемост е около 70%. Индивидуалната вероятност за оцеляване зависи от стадия на рака, възможността за пълното му отстраняване чрез операция и общото здравословно състояние на пациента. В световен мащаб колоректалният рак е третият най-често срещан вид рак, като представлява около 10% от всички случаи. През 2018 г. са регистрирани 1,09 милиона нови случая и 551 000 смъртни случая от болестта. По-често се среща в развитите страни, където се откриват над 65% от случаите, и е по-рядък при жените, отколкото при мъжете.
Признаците и симптомите на колоректалния рак зависят от местоположението на тумора в червата и от това дали се е разпространил другаде в тялото (метастази), като класическите предупредителни знаци включват: влошаващ се запек, кръв в изпражненията, намаляване на дебелината на изпражненията, загуба на апетит, отслабване и гадене или повръщане при хора над 50 години, като около 50% от болните нямат симптоми; ректалното кървене или анемията са високорискови симптоми при хора над 50 години, а отслабването и промените в изхожданията са тревожни, ако са свързани с ректално кървене.
75–95% от случаите на колоректален рак се срещат при хора с малък или никакъв генетичен риск. Рисковите фактори включват напреднала възраст, мъжки пол, висок прием на мазнини, захар, алкохол, червено месо, преработени меса, затлъстяване, тютюнопушене и липса на физическа активност. Като допълнителен рисков фактор някои калкулатори за преживяемост на ректален рак отчитат и расата, но има опасения, че това може да доведе до неравенство в клиничните решения. Около 10% от случаите са свързани с недостатъчна физическа активност. Рискът от алкохол се увеличава при повече от една напитка на ден. Пиенето на пет чаши вода дневно е свързано с намален риск от колоректален рак и аденоматозни полипи. Консумацията на млечни продукти, като мляко, има защитен ефект срещу колоректален рак. Streptococcus gallolyticus е свързан с колоректален рак. Някои щамове на Streptococcus bovis/Streptococcus equinus комплекс се консумират ежедневно от милиони хора и може да са безопасни. 25 до 80% от хората с бактериемия от Streptococcus bovis/gallolyticus имат съпътстващи колоректални тумори. Серопревалентността на Streptococcus bovis/gallolyticus се разглежда като потенциален маркер за ранно предсказване на подлежащо чревно увреждане при високорискови групи. Предполага се, че наличието на антитела към Streptococcus bovis/gallolyticus или самите антигени в кръвта може да служи като маркер за канцерогенеза в дебелото черво.
Патогенни щамове на Escherichia coli могат да увеличат риска от колоректален рак чрез производството на генотоксичния метаболит колибактин.
Възпалителни заболявания на червата
Хората с възпалителни заболявания на червата (улцерозен колит и болест на Крон) са с повишен риск от рак на дебелото черво. Рискът се увеличава с продължителността на заболяването и тежестта на възпалението. При тези високорискови групи се препоръчва профилактика с аспирин и редовни колоноскопии. Ендоскопското наблюдение при тази група може да намали развитието на колоректален рак чрез ранна диагноза и да намали риска от смърт. Хората с възпалителни заболявания на червата представляват по-малко от 2% от случаите на рак на дебелото черво годишно. При болест на Крон (с ангажиране на дебелото черво) 2% развиват колоректален рак след 10 години, 8% след 20 години и 18% след 30 години. При улцерозен колит около 16% развиват прекурсор на рак или рак на дебелото черво за 30 години.
Генетика
Хората с фамилна анамнеза при двама или повече роднини от първа степен (като родител или брат/сестра) имат 2 до 3 пъти по-висок риск от заболяване, като тази група представлява около 20% от всички случаи. Няколко генетични синдрома също са свързани с по-високи нива на колоректален рак. Най-честият от тях е наследственият неполипозен колоректален рак (HNPCC или синдром на Линч), който се среща при около 3% от хората с колоректален рак. Други синдроми, силно свързани с колоректален рак, включват синдром на Гарднър и фамилна аденоматозна полипоза (FAP). При тези синдроми ракът почти винаги се развива и представлява 1% от случаите. Пълна проктоколектомия може да се препоръча при хора с FAP като превантивна мярка поради високия риск от злокачествено заболяване. Само колектомия (отстраняване на дебелото черво) може да не е достатъчна, тъй като остава висок риск от рак на ректума, ако ректумът не бъде премахнат. Най-честият полипозен синдром, засягащ дебелото черво, е сертифицираният полипозен синдром, който е свързан с 25–40% риск от колоректален рак.
Мутации в двойка гени (POLE и POLD1) са свързани с фамилен рак на дебелото черво.
Повечето смъртни случаи от рак на дебелото черво са свързани с метастатично заболяване. Изолиран е ген, който изглежда допринася за потенциала за метастатично заболяване – MACC1 (metastasis associated in colon cancer 1). Това е транскрипционен фактор, който влияе върху експресията на хепатоцитния растежен фактор. Този ген е свързан с пролиферация, инвазия и разпространение на клетки на рак на дебелото черво в клетъчни култури, както и с растеж и метастази на тумори при мишки. MACC1 може да бъде потенциална цел за интервенция при рак, но това трябва да се потвърди с клинични проучвания.
Епигенетични фактори, като абнормна метилация на ДНК на промотори на туморни супресори, играят роля в развитието на колоректален рак.
Ашкеназите имат с 6% по-висок риск от развитие на аденоми и след това рак на дебелото черво поради по-чести мутации в APC гена.
Диета
Свързана с диета с високо съдържание на мазнини, повишените нива на жлъчни киселини изглежда увеличават риска от колоректален рак. Особено дезоксихоловата киселина е повишена в съдържанието на дебелото черво при хора, които консумират много мазнини. В популации с висока честота на колоректален рак, концентрациите на жлъчни киселини в изпражненията, особено дезоксихоловата киселина, са по-високи.
Мета-анализ от 2025 г. за връзката между концентрациите на жлъчни киселини в изпражненията и развитието и прогресията на колоректалния рак установява, че по-високите концентрации на жлъчните киселини холева и хенодезоксихолева киселина са свързани с по-висок риск и по-голяма честота на колоректрален рак.
Колоректалният рак е заболяване, което произхожда от епителните клетки, покриващи дебелото черво или ректума на храносмилателния тракт, най-често в резултат на генетични мутации в Wnt сигналния път, които увеличават сигналната активност. Wnt сигналният път обикновено играе важна роля за нормалната функция на тези клетки, включително поддържането на тази лигавица. Мутациите могат да бъдат наследствени или придобити и най-вероятно възникват в стволовите клетки на чревните крипти. Най-често мутиралият ген при всички случаи на колоректален рак е APC, който произвежда APC протеин. Този протеин предотвратява натрупването на β-катенин. Без APC, β-катенинът се натрупва в големи количества, преминава в ядрото, свързва се с ДНК и активира транскрипцията на протоонкогени. Тези гени обикновено са важни за обновяването и диференциацията на стволовите клетки, но когато се експресират прекомерно, могат да причинят рак. Докато APC е мутирал в повечето случаи на рак на дебелото черво, някои ракови заболявания имат повишен β-катенин поради мутации в самия β-катенин (CTNNB1), които блокират разграждането му, или поради мутации в други гени с подобна функция като APC, като AXIN1, AXIN2, TCF7L2 или NKD1.
Освен дефектите в Wnt сигналния път, трябва да настъпят и други мутации, за да стане клетката ракова. Протеинът p53, произвеждан от гена TP53, обикновено следи клетъчното делене и предизвиква програмирана клетъчна смърт, ако има дефекти в Wnt пътя. В крайна сметка, клетъчна линия придобива мутация в TP53 и трансформира тъканта от доброкачествен епителен тумор в инвазивен рак. Понякога генът за p53 не е мутирал, но друг защитен протеин, наречен BAX, е мутирал вместо това.
Други протеини, отговорни за програмирана клетъчна смърт, които често са деактивирани при колоректален рак, са TGF-β и DCC (Deleted in Colorectal Cancer). TGF-β има деактивираща мутация в поне половината от случаите на колоректален рак. Понякога TGF-β не е деактивиран, но надолу по веригата протеинът SMAD е деактивиран. DCC често има изтрит сегмент от хромозома при колоректален рак.
Около 70% от всички човешки гени се експресират при колоректален рак, като малко над 1% имат повишена експресия в сравнение с други видове рак. Някои гени са онкогени: те са свръхекспресирани при колоректален рак. Например, гените, кодиращи протеините KRAS, RAF и PI3K, които обикновено стимулират клетъчното делене в отговор на растежни фактори, могат да придобият мутации, водещи до свръхактивиране на клетъчната пролиферация. Хронологичният ред на мутациите понякога е важен – ако преди това е настъпила мутация в APC, първична мутация в KRAS често води до рак, вместо до самоограничаваща се хиперпластична или гранична лезия. PTEN, туморен супресор, обикновено инхибира PI3K, но понякога може да бъде мутирал и деактивиран.
Обширен геномен анализ показва, че колоректалните карциноми могат да се категоризират като хипермутирани и нехипермутирани туморни типове. Освен описаните по-горе мутации, нехипермутираните проби съдържат и мутации в CTNNB1, FAM123B, SOX9, ATM и ARID1A. Хипермутиралите тумори показват мутации във форми на ACVR2A, TGFBR2, MSH3, MSH6, SLC9A9, TCF7L2 и BRAF. Общата тема между тези гени и при двата типа тумори е участието им в Wnt и TGF-β сигналните пътища, което води до повишена активност на MYC – централен фактор в колоректалния рак.
Туморите с дефицит на mismatch repair (MMR) се характеризират с относително голям брой тандемни повторения на полинуклеотиди. Това се дължи на дефицит на MMR протеини – обикновено причинен от епигенетично заглушаване или наследствени мутации (например синдром на Линч). 15 до 18% от туморите на колоректален рак имат MMR дефицити, като 3% се развиват поради синдрома на Линч. Ролята на системата за поправка на несъответствията е да защитава целостта на генетичния материал в клетките (т.е. да открива и коригира грешки). Следователно, дефицитът на MMR протеини може да доведе до невъзможност за откриване и поправка на генетични увреждания, което позволява да настъпят допълнителни мутации, причиняващи рак, и прогресия на колоректалния рак.
Последователността от полип към рак е класическият модел на патогенезата на колоректалния рак. В тази аденома-карцинома последователност нормалните епителни клетки прогресират до диспластични клетки като аденоми, а след това до карцином чрез процес на прогресивна генетична мутация. Централни за тази последователност са генетичните мутации, епигенетичните промени и локалните възпалителни процеси. Тази последователност може да се използва като основна рамка за илюстриране как специфични молекулярни промени водят до различни подтипове рак.
Дефектни полета
Терминът „поле на канцеризация“ е използван за пръв път през 1953 г., за да опише област или „поле“ от епител, което е било предварително променено (от процеси, които по онова време до голяма степен са били неизвестни) така, че да бъде предразположено към развитие на рак. Оттогава насам термините „поле на канцеризация“, „карциногенеза на полето“, „дефект на полето“ и „ефект на полето“ се използват за описание на предракови или пренеопластични тъкани, в които е вероятно да възникнат нови ракови образувания.
Полевите дефекти играят важна роля в прогресията на колоректалния рак.
Както обаче отбелязва Рубин, „огромното мнозинство от изследванията в областта на рака са извършени върху добре дефинирани тумори in vivo или върху отделни неопластични огнища in vitro. Въпреки това има данни, че над 80% от соматичните мутации, открити в колоректални тумори с мутационен фенотип при хора, се появяват преди началото на терминалната клонална експанзия.“ По подобен начин, Фогелщайн и съавт. посочват, че повече от половината соматични мутации, идентифицирани в тумори, са възникнали в пренеопластичната фаза (в полеви дефект), по време на растежа на привидно нормални клетки. Също така, епигенетични изменения, присъстващи в туморите, може да са се появили в пренеопластични полеви дефекти.
Разширеното разбиране на ефекта на полето е наречено „етиологичен ефект на полето“, който включва не само молекулярните и патологичните промени в пренеопластичните клетки, но и влиянието на външни екологични фактори и молекулярните промени в локалната микроок среда върху неопластичното развитие – от инициирането на тумора до смъртта.
Епигенетика
Както е описано от Фогелщайн и съавт., средният случай на рак на дебелото черво съдържа само 1 или 2 мутации в онкогени и от 1 до 5 мутации в тумор-супресорни гени (заедно наричани „водещи мутации“), както и около 60 допълнителни „пътнически“ мутации. Онкогените и тумор-супресорните гени са добре проучени и са разгледани по-горе в раздела Патогенеза.
Епигенетичните изменения са много по-чести при колоректален рак, отколкото генетичните (мутационни) промени. Епигенетичните изменения, за разлика от мутациите, променят експресията на белтъци без да променят ДНК последователността. Един често срещан тип епигенетична промяна при колоректален рак е промяната в нивото на експресия на определени микроРНК (miRNAs). МикроРНК са малки РНК молекули, които се свързват с 3′-нетранслирани региони на своите мишени – информационни РНК (mRNAs) – и потискат транслацията на протеини. Намалената или увеличената регулация на микроРНК представлява епигенетична промяна, тъй като тази регулация не включва директна промяна в ДНК последователността.
МикроРНК играят важна роля като епигенетични фактори при колоректалния рак – при този вид рак са установени значителни промени в 164 микроРНК. Една микроРНК може да регулира средно около 300 гена. Смята се, че около 60% от човешките белтъчно-кодиращи гени са под епигенетичен контрол чрез микроРНК. Например, miRNA-143 е понижена в 88% от случаите на колоректален рак, а това води до повишена експресия на нейните мишени – онкогена KRAS и ензима за метилиране на ДНК DNMT3A.
Освен чрез промяна в експресията на микроРНК, други често срещани епигенетични механизми в раковите заболявания включват директна хиперметилация или хипометилация на CpG острови в белтъчно-кодиращите гени, както и промени в хистони и хромозомна архитектура, които влияят върху генната експресия. Например, 147 хиперметилации и 27 хипометилации на белтъчно-кодиращи гени са често свързвани с колоректален рак. От тези хиперметилирани гени, 10 са хиперметилирани в 100% от случаите на рак на дебелото черво, а много други – в над 50% от случаите. Освен това, 11 хиперметилации и 96 хипометилации на микроРНК също се свързват с колоректален рак. Абнормната (аномална) метилация се появява естествено с напредването на възрастта и рискът от рак на дебелото черво нараства с възрастта. Източникът и причината за тази възрастово свързана метилация все още са неизвестни. Приблизително половината от гените, които показват възрастово-зависими метилационни промени, съвпадат с гени, за които се знае, че участват в развитието на колоректален рак. Тези открития може да обясняват защо възрастта е значим рисков фактор за заболяването.
Епигенетичното намаляване на експресията на ензими, отговорни за репарация на ДНК, може да доведе до геномна и епигеномна нестабилност, характерна за рака. Както е обобщено в статиите за канцерогенеза и неоплазия, при спорадичните ракови заболявания, дефицитът на ДНК репарация понякога се дължи на мутация в съответен ген, но много по-често – на епигенетични промени, които потискат или изключват експресията на гени, отговорни за ДНК репарация.
Епигенетичните изменения, свързани с развитието на колоректален рак, може да повлияят и на отговора към химиотерапията.
Геномика и епигеномика
Класификацията на консенсусните молекулярни подтипове (CMS) на колоректалния рак е въведена за първи път през 2015 г. Тя се счита за най-стабилната и надеждна система за класификация на този тип рак, която предлага ясно биологично обяснение и основа за бъдещо клинично стратифициране и целенасочени терапии, базирани на подтиповете.
През 2021 г. е предложена нова епигеномно-базирана класификация (EpiC) на колоректалния рак, която включва 4 подтипа на енхансъри (регулаторни елементи) при пациенти с CRC. Хроматиновите състояния са охарактеризирани чрез 6 хистонни модификации, за да се идентифицират EpiC подтиповете. Комбиниран терапевтичен подход, основан на вече въведените CMS подтипове и EpiC подтиповете, би могъл значително да подобри настоящите стратегии за лечение.
Образни изследвания
Колоректалният рак понякога се открива първоначално при компютърна томография (КТ скенер).
Наличието на метастази се определя чрез КТ скенер на гръдния кош, корема и таза. В определени случаи могат да се използват и други методи за образна диагностика, като PET сканиране и ядрено-магнитен резонанс (MRI). ЯМР е особено полезен за определяне на локалния стадий на тумора и за планиране на най-подходящия хирургичен подход.
ЯМР се извършва също и след завършване на неоадювантна химио-лъчетерапия, за да се идентифицират пациенти, постигнали пълен отговор към лечението. Пациенти, при които се установи пълен отговор както на ЯМР, така и при ендоскопия, може да не се нуждаят от хирургично отстраняване на тумора и така да избегнат ненужни хирургични усложнения и следоперативна заболеваемост.
Пациенти, избрани за нехирургично лечение на ректален рак, трябва да преминават през периодични ЯМР прегледи, физикални изследвания и ендоскопии, за да се открие евентуално повторно развитие на тумора – нещо, което се случва при малък брой от тези пациенти. Когато се появи локален рецидив, периодичното проследяване може да го открие в ранен стадий, когато все още е лечим чрез спасителна операция.
Освен това, след химио-лъчетерапия може да се определят степени на туморна регресия на ЯМР (mrTRG), които се сравняват с патологичните степени на регресия (pTRG) и корелират с дългосрочната преживяемостна пациентите.
Хистопатология
Хистопатологични характеристики
Хистопатологичните характеристики на тумора се определят чрез анализ на тъкан, взета по време на биопсия или хирургична интервенция. Патологичната диагноза съдържа описание на микроскопските характеристики на туморната тъкан, включително както самите туморни клетки, така и начина, по който туморът нахлува в здравите тъкани, както и дали изглежда, че туморът е напълно отстранен.
Най-честата форма на рак на дебелото черво е аденокарцином, който представлява между 95% и 98% от всички случаи на колоректален рак. Други, по-редки видове включват лимфом, аденосквамозен карцином и сквамозноклетъчен карцином. Някои подтипове са по-агресивни.
При неясни случаи може да се използва имунохистохимия за по-точна диагноза.
Стадиране
Стадирането на рака се базира както на образни, така и на хистологични находки. Както при повечето други видове рак, стадирането се извършва по TNM системата, която отчита:
-
колко е разпространен първичният тумор,
-
наличие на метастази в лимфни възли,
-
наличие на отдалечени метастази в други органи.
Смята се, че около половината от случаите на колоректален рак се дължат на фактори, свързани с начина на живот, а около една четвърт от всички случаи могат да бъдат предотвратени. Повишеният контрол, физическата активност, консумацията на храни с високо съдържание на фибри, отказът от тютюнопушене и ограничаването на алкохола намаляват риска.
Начин на живот
Фактори на начина на живот с доказан риск включват липсата на физическа активност, тютюнопушене, употреба на алкохол и затлъстяване. Рискът от колоректален рак може да се намали чрез поддържане на нормално телесно тегло чрез достатъчна физическа активност и здравословно хранене.
Настоящите изследвания последователно свързват консумацията на червено и преработено месо с по-висок риск от заболяването. От 70-те години насам, препоръките за диета с цел превенция включват увеличаване на приема на пълнозърнести храни, плодове и зеленчуци, както и намаляване на червеното и преработено месо. Въпреки това, мащабни проспективни проучвания не показват значим защитен ефект, а поради множествените причини за рак и сложността на диетичните проучвания, остава неясно дали конкретна диетична намеса има значим ефект.
Консумацията на алкохолни напитки и преработено месо увеличава риска от колоректален рак.
Доклад на СЗО от 2014 г. отбелязва, че диетичните фибри могат да имат превантивен ефект, но повечето проучвания дотогава не са изследвали връзката. Преглед от 2019 г. открива доказателства за полза от фибрите и пълнозърнестите храни. Според Световния фонд за изследване на рака, ползата от фибрите е „вероятна“ (към 2017 г.), а преглед от 2022 г. определя връзката като с „убедителни доказателства“.
Физическата активност се препоръчва. Тя е свързана с умерено намален риск от рак на дебелото, но не и на правото черво. Високата физическа активност намалява риска с около 21%. Продължителното заседяване е свързано с по-висока смъртност от рак на дебелото черво. Упражненията не елиминират риска, но го намаляват.
Медикаменти и хранителни добавки
Аспирин и целекоксиб намаляват риска при хора с висок риск. Аспирин се препоръчва за хора на възраст 50–60 години без повишен риск от кървене и с риск от сърдечно-съдови заболявания, но не и за хора със среден риск.
Има слаби доказателства в полза на калциеви добавки, но не достатъчно за препоръка.
Адекватният прием на витамин D и нормални нива в кръвта са свързани с по-нисък риск от рак на дебелото черво.
Скрининг
Повече от 80% от колоректалните карциноми произхождат от аденоматозни полипи, затова скринингът е ефективен за ранно откриване и превенция. Чрез скрининг диагнозата се поставя 2–3 години преди появата на симптоми. Откритите полипи могат да се отстранят чрез колоноскопия или сигмоидоскопия, предотвратявайки развитието на рак. Скринингът може да намали смъртността с до 60%.
Основни методи: колоноскопия, тест за окултно кървене в изпражненията (FOBT), и флексибилна сигмоидоскопия. Сигмоидоскопията не обхваща дясната част на дебелото черво (където се откриват 42% от случаите), но има най-силни доказателства за намаляване на общата смъртност.
FOBT се препоръчва на всеки 1-2 години. Ако резултатът е положителен, се извършва колоноскопия. FOBT намалява смъртността с 16%, а при участниците в скрининга — с до 23%. Имунологичните тестове са по-точни и не изискват диетични ограничения, но праговете в някои страни (като Англия) може да пропуснат над половината случаи.
Други методи: виртуална колоноскопия и FIT-DNA (ДНК тест на изпражненията). Виртуалната колоноскопия е толкова добра, колкото и стандартната за откриване на рак и големи аденоми, но не позволява премахване на образувания. FIT-DNA има повече фалшиви положителни резултати и следователно повече странични ефекти. Нужни са още проучвания относно оптималния интервал между тестовете.
Препоръки
В САЩ скринингът обикновено започва между 50 и 75 г. Американското онкологично общество препоръчва от 45 г. За хора между 76–85 г., решението трябва да е индивидуализирано. При висок риск скринингът започва около 40 г.
Методи: изследване на изпражненията на всеки 2 години, сигмоидоскопия на всеки 10 години с имунохимичен тест на всеки 2 години, или колоноскопия на всеки 10 години. Колоноскопията открива повече случаи, но е по-скъпа и с повече усложнения. При нормална колоноскопия не се препоръчва повторен скрининг в следващите 10 години. Над 75 г. или с живот под 10 години — не се препоръчва. Едва след 10 години се наблюдава полза при 1 от 1000 души.
В Канада: при хора на възраст 50–75 г. с нормален риск се препоръчва имунохимичен тест или FOBT на всеки 2 години, или сигмоидоскопия на всеки 10 години. Колоноскопията не е предпочитана.
Много страни имат национални програми за скрининг — напр. Великобритания, Австралия, Нидерландия, Хонконг и Тайван. В Обединеното кралство програмата е за хора на възраст 60–74 г., с FIT на всеки 2 години. При положителен резултат се извършва изследване на чревната тъкан и отстраняване на потенциално злокачествени образувания. Такава програма вече има и в България.
Лечението на колоректалния рак може да бъде насочено към излекуване или облекчаване (палиация). Решението коя цел да се преследва зависи от различни фактори, включително здравословното състояние и предпочитанията на пациента, както и стадия на тумора. Оценката от мултидисциплинарни екипи е ключова част от определянето на това дали пациентът е подходящ за хирургична намеса. Когато колоректалният рак бъде открит рано, хирургичното лечение може да бъде изцелително. В по-късните стадии (когато вече има метастази) това е по-малко вероятно и лечението често е насочено към палиация – облекчаване на симптомите, причинени от тумора, и осигуряване на максимален комфорт за пациента.
Хирургия
В ранен стадий колоректалният рак може да бъде отстранен по време на колоноскопия чрез някой от няколко метода, включително ендоскопска мукозна резекция или ендоскопска субмукозна дисекция. Ендоскопска резекция е възможна, ако вероятността за метастази в лимфни възли е ниска и размерът и разположението на тумора позволяват премахване „en bloc“ (в един блок).
При хора с локализиран рак предпочитаното лечение е пълно хирургично отстраняване с достатъчно широки граници с цел постигане на излекуване. Предпочитаният метод е частична колектомия (или проктоколектомия при ректални лезии), при която се премахва засегнатата част на дебелото или правото черво, заедно с част от мезоколона и кръвоснабдяването, за да се улесни отстраняването на лимфните възли.
Операцията може да се извърши чрез отворена лапаротомия или лапароскопски, в зависимост от индивидуалните характеристики на пациента и особеностите на лезията. След това дебелото черво може да бъде свързано отново, или на пациента може да бъде направена колостомия.
Ако има само няколко метастази в черния дроб или белите дробове, те също могат да бъдат премахнати. Химиотерапия може да се използва преди операция, за да се намали размерът на тумора преди неговото отстраняване. Двете най-чести места за рецидив на колоректален рак са черният дроб и белите дробове. При перитонеална карциноматоза може да се използва циторедуктивна хирургия, понякога в комбинация с HIPEC (хипертермична интраперитонеална химиотерапия), с цел отстраняване на рака.
Химиотерапия
При рак както на дебелото черво, така и на правото черво, химиотерапия може да се използва в допълнение към хирургичното лечение в определени случаи. Решението дали да се добави химиотерапия при лечението на колоректален рак зависи от стадия на заболяването.
При рак на дебелото черво в стадий I не се прилага химиотерапия – хирургичното лечение е окончателно. Ролята на химиотерапията при стадий II е спорна и обикновено не се прилага, освен ако не са налице рискови фактори като тумор T4, недиференциран тумор, съдова или периневрална инвазия или недостатъчно изследвани лимфни възли. Известно е също, че хора с генетични нарушения в т.нар. mismatch repair гени не се повлияват от химиотерапия. При стадий III и IV на рак на дебелото черво химиотерапията е неразделна част от лечението.
Ако ракът се е разпространил към лимфни възли или към отдалечени органи – което съответства на стадии III и IV – добавянето на химиотерапевтични средства като флуороурацил, капецитабин или оксалиплатин увеличава продължителността на живота. Ако лимфните възли не съдържат рак, ползата от химиотерапията е спорна. При широко метастазирал или нерезектабилен рак лечението е палиативно. В този случай обикновено се използват различни химиотерапевтични медикаменти.
Химиотерапевтичните лекарства, използвани при това състояние, могат да включват капецитабин, флуороурацил, иринотекан, оксалиплатин и UFT. Капецитабин и флуороурацил са взаимозаменяеми – капецитабин се приема през устата, а флуороурацил се прилага венозно. Някои от използваните схеми при колоректален рак са CAPOX, FOLFOX, FOLFOXIRI и FOLFIRI.
Антиангиогенни лекарства като бевацизумаб често се добавят като част от първа линия на терапия. Друга група лекарства, използвани като втора линия, са инхибиторите на рецепторите за епидермален растежен фактор (EGFR), от които три са одобрени от FDA: афлиберцепт, цетуксимаб и панитумумаб.
Основната разлика в подхода при лечението на ректален рак в ранен стадий е включването на лъчетерапия. Често тя се прилага в комбинация с химиотерапия като неоадювантно лечение с цел да се направи туморът операбилен и да се избегне поставяне на колостома. Това обаче невинаги е възможно при нискоразположени тумори, при които може да се наложи постоянна колостома. Ректалният рак в стадий IV се лекува по подобен начин на стадий IV на рак на дебелото черво.
Колоректален рак в стадий IV с перитонеална карциноматоза може да бъде лекуван с HIPEC (хипертермична интраперитонеална химиотерапия) в комбинация с циторедуктивна хирургия при някои пациенти. Също така, при T4 колоректален рак HIPEC може да се използва с цел предотвратяване на рецидиви.
Лъчетерапия
Комбинирането на лъчетерапия и химиотерапия може да бъде полезно при ректален рак, но при някои пациенти химиорадиотерапията увеличава токсичността по време на лечението, без да показва по-добра преживяемост в сравнение с лъчетерапията самостоятелно. Все пак, тя е свързана с по-нисък риск от локален рецидив. При плоскоклетъчен карцином на аналния канал, хеморадиотерапия с 5-FU и митомицин С е предпочитана пред само лъчелечение, като предлага по-добри резултати по отношение на преживяемостта, но с повишен риск от хематологична токсичност.
Лъчетерапията не е стандартна при рак на дебелото черво поради чувствителността на червата към радиация. Страничните ефекти от лъчетерапията включват: остри кожни реакции (27%), късни кожни усложнения (17%), остри гастроинтестинални токсичности (14%), късни гастроинтестинални усложнения (27%) и късна тазова радиационна болест (1–10%), напр. необратима лумбосакрална плексопатия.
Както и при химиотерапията, лъчетерапия може да се използва като неоадювант при стадии T3 и T4 на ректален рак, с цел намаляване на размера или стадия на тумора и намаляване на риска от локален рецидив. При локално напреднал ректален рак неоадювантната хеморадиотерапия е стандартна терапия. Освен това, когато операцията не е възможна, лъчетерапията може да се използва за лечение на метастази в белия дроб, които се развиват при 10–15% от пациентите с колоректален рак.
Имунотерапия
Имунотерапия с инхибитори на имунни контролни точки е ефективна при вид колоректален рак с дефицит в DNA mismatch repair (MMR) и микросателитна нестабилност (MSI). Пембролизумаб е одобрен за лечение на напреднали тумори на колоректален рак с MMR дефицит, при които стандартното лечение е неуспешно. Въпреки това, повечето пациенти, които първоначално се повлияват, влошават състоянието си след месеци или години.
Палиативни грижи
Палиативната грижа може да се прилага паралелно с онкологичното лечение и се препоръчва при пациенти с напреднал рак на дебелото черво или значителни симптоми. Участието на палиативен екип може да подобри качеството на живот както на пациента, така и на неговото семейство чрез облекчаване на симптомите, намаляване на тревожността и предотвратяване на ненужни хоспитализации.
При нелечим колоректален рак палиативната грижа може да включва процедури, които облекчават симптомите и усложненията от рака, без да лекуват самия рак, с цел подобряване на качеството на живот. Хирургичните възможности могат да включват нерадикално отстраняване на част от тумора, байпас на чревен сегмент или поставяне на стент. Тези интервенции се прилагат за облекчаване на симптоми като кръвотечение, болка в корема и чревна непроходимост. Нехирургичните методи за симптоматично лечение включват лъчетерапия за намаляване на размера на тумора и обезболяващи медикаменти.
Освен медицинската намеса, се прилагат различни психосоциални интервенции за справяне с психосоциалните затруднения при пациенти с колоректален рак (КРР). Депресията и тревожността са силно разпространени сред хората с такава диагноза, поради което психосоциалните подходи могат да облекчат психологическия дистрес. Много пациенти продължават да изпитват симптоми на тревожност и депресия и след приключване на лечението, независимо от неговия изход. Освен това, обществените стигми, свързани с колоректалния рак, създават допълнителни психосоциални предизвикателства за пациентите и техните семейства.
Депресия и тревожност
Пациентите с колоректален рак имат с 51% по-висок риск от развитие на депресия в сравнение с хора без заболяването. Освен това, те са изложени на висок риск от тежка тревожност, ниска самооценка, негативна представа за себе си и социална тревожност.
Дистрес след лечението
Независимо от изхода от лечението, много пациенти с КРР продължават да изпитват тревожност, депресия и дистрес.
Оцеляването след КРР често изисква значителни промени в начина на живот. Следоперативните затруднения могат да включват стома, чревни проблеми, инконтиненция, неприятна миризма и промени в сексуалната функция. Тези промени могат да доведат до изкривена представа за тялото, социална тревожност, депресия и дистрес – всички те допринасят за понижено качество на живот.
Колоректалният рак е втората водеща причина за смъртност от рак в световен мащаб. Преминаването към палиативни грижи и изправянето пред смъртността могат да бъдат дълбоко травматични преживявания както за пациентите, така и за техните близки.
Стигма
Колоректалният рак носи силна обществена стигма и може да предизвика чувство на отвращение у пациентите, здравните специалисти, семейството, интимните партньори и обществото като цяло. Пациентите със стома са особено уязвими на стигматизация поради неизбежни миризми, газове и неприятни звуци от стомните торбички. Освен това, свързани рискови фактори като нездравословно хранене, употреба на алкохол и липса на физическа активност често водят до негативни предположения и обвинения към самите пациенти. Осъждането от страна на околните, заедно с вътрешно усещане за вина и срам, могат да имат отрицателно въздействие върху самооценката, социалните взаимоотношения и качеството на живот.
Методи за психологическа помощ
Най-ефективни за намаляване на тревожността и депресията при пациенти с КРР се считат личните срещи с терапевт, практики, свързани с тялото, ума и духа, както и групови сесии за подкрепа. Освен това, прилагани са упражнения с водене на дневник и телефонна терапия. Макар и с по-ниска ефективност, тези дистанционни интервенции са икономически достъпни и също така доказано намаляват симптомите на депресия и тревожност при пациенти с КРР.
Националната мрежа за борба с рака на САЩ (U.S. National Comprehensive Cancer Network) и Американското дружество по клинична онкология (American Society of Clinical Oncology) предоставят насоки за последващо наблюдение при пациенти с рак на дебелото черво.
Препоръчва се снемане на медицинска анамнеза и физикален преглед на всеки 3 до 6 месеца през първите 2 години, а след това – на всеки 6 месеца до края на петата година. Измерването на нивата на карциноембрионален антиген (CEA) в кръвта следва същия график, но се препоръчва само за хора с тумори от стадий T2 или по-висок, които са кандидати за последващи лечебни интервенции.
Скенер (CT) на гръдния кош, корема и таза може да се обмисли веднъж годишно през първите 3 години при пациенти с висок риск от рецидив (например при ниско диференцирани тумори или при наличие на венозна или лимфна инвазия), които са кандидати за потенциално излекуваща хирургия.
Колоноскопия може да се направи една година след лечението, освен ако не е била възможна при първоначалната диагностика поради запушваща маса – в такъв случай тя трябва да се извърши в рамките на 3 до 6 месеца. Ако се открие вилообразен полип, полип с големина над 1 сантиметър или дисплазия с висока степен, колоноскопията се повтаря след 3 години, а след това – на всеки 5 години. При други аномалии колоноскопията може да се повтори след 1 година.
Рутинната употреба на ПЕТ скенер, ултразвук, рентгенография на гръдния кош, пълна кръвна картина или чернодробни функционални изследвания не се препоръчва.
При хора, преминали през излекуваща хирургия или адювантна терапия (или и двете) за неметастатичен колоректален рак, интензивното проследяване и честите прегледи не са показали допълнителни ползи по отношение на преживяемостта.
Около 600 гена са свързани с прогнозата при колоректален рак. Това включва както неблагоприятни гени, при които високата експресия се свързва с по-лоша прогноза – например гена за топлинов шоков протеин 70 kDa (HSPA1A), така и благоприятни гени, при които високата експресия се асоциира с по-добра преживяемост – например гена за предполагаемата РНК-свързваща протеин 3 (RBM3). Прогнозата също така се свързва с лошата точност на апарата за сплайсинг на пре-mRNA, което води до голям брой отклоняващи се алтернативни сплайсинг варианти.
Честота на рецидивите
Средната честота на рецидив в рамките на пет години при хора с рак на дебелото черво, при които операцията е била успешна, е:
-
5% за стадии I,
-
12% за стадии II,
-
33% за стадии III.
В зависимост от броя на рисковите фактори, тази честота варира от:
-
9–22% при стадии II,
-
17–44% при стадии III.
При ректален рак, средната честота на рецидив в рамките на пет години след успешна хирургия е:
-
9% за стадии 0 (след предлечение),
-
8% за стадии I,
-
18% за стадии II,
-
34% за стадии III.
Рискът от далечни метастази при ректален рак според броя на рисковите фактори (0–2) е:
-
4–11% при стадии 0,
-
6–12% при стадии I,
-
11–28% при стадии II,
-
15–43% при стадии III.
Честотата на рецидивите е намаляла през последните десетилетия благодарение на подобренията в лечението на колоректалния рак. Рискът от рецидив след петгодишно проследяване остава много нисък.
Преживяемост
В Европа петгодишната преживяемост при колоректален рак е под 60%. В развитите страни около една трета от заболелите умират от болестта.
Преживяемостта зависи пряко от ранното откриване и от вида на рака, но като цяло е ниска при симптоматични случаи, тъй като обикновено са в напреднал стадий. Преживяемостта при ранно откриване е около пет пъти по-висока отколкото при късно диагностицирани случаи.
-
При пациенти с тумор, който не е преминал мускуларис мукозата (стадий Tis, N0, M0), петгодишната преживяемост е 100%.
-
При инвазивен рак от стадий T1 (в субмукозата) или T2 (в мускулатурата), преживяемостта е около 90%.
-
При по-инвазивни тумори без засягане на лимфни възли (T3–4, N0, M0), преживяемостта е около 70%.
-
При засягане на регионални лимфни възли (всеки T, N1–3, M0), преживяемостта е около 40%.
-
При далечни метастази (всеки T, всеки N, M1), прогнозата е лоша, като петгодишната преживяемост варира от под 5% до 31%.
Петгодишната обща преживяемост (OS) при ректален рак след съвременно предоперативно лечение и операция е:
-
90% за стадий 0,
-
86% за стадий I,
-
78% за стадий II,
-
67% за стадий III, според национално популационно изследване.
Живот след лечението
Влиянието на колоректалния рак върху преживелите варира значително, но често се налага адаптация към физическите и психични последици от болестта и лечението.
Чести проблеми включват:
-
инконтиненция,
-
сексуална дисфункция,
-
трудности с грижата за стома,
-
страх от рецидив на рака.
Систематичен качествен преглед, публикуван през 2021 г., подчертава три основни фактора, които влияят върху адаптацията към живот след колоректален рак:
-
Механизми за подкрепа,
-
Тежест на късните ефекти от лечението,
-
Психосоциална адаптация.
Поради това е от съществено значение хората да получат подходяща подкрепа, която да подпомогне адаптацията им към живота след лечението.
В света над 1 милион души годишно се разболяват от колоректален рак, което води до около 715 000 смъртни случая към 2010 г., спрямо 490 000 през 1990 г.
Към 2012 г. това е втората най-честа форма на рак при жените (9.2% от диагнозите) и третата при мъжете (10.0%), като е четвъртата най-честа причина за смърт от рак след рака на белия дроб, стомаха и черния дроб. Колоректалният рак е по-често срещан в развитите страни, отколкото в развиващите се. Разпространението му в световен мащаб варира десетократно – с най-високи нива в Австралия, Нова Зеландия, Европа и САЩ и най-ниски в Африка и Южна Централна Азия.
Съединени Американски Щати
През 2022 г. се очакваше честотата на колоректален рак в САЩ да бъде около 151 000 нови случая при възрастни, включително над 106 000 нови случая на рак на дебелото черво (около 54 000 мъже и 52 000 жени) и около 45 000 нови случая на рак на ректума. От 80-те години насам честотата на колоректалния рак е намаляла – с около 2% годишно между 2014 и 2018 г. при възрастни над 50 години, главно поради подобрен скрининг.
Обаче, честотата на заболяването нараства сред хора на възраст между 25 и 50 години. В началото на 2023 г. Американското онкологично дружество (ACS) съобщи, че през 2019 г. 20% от диагнозите на рак на дебелото черво са били при пациенти под 55 години – приблизително двойно спрямо 1995 г. Освен това, честотата на напреднал рак е нараствала с около 3% годишно при хора под 50 години. Прогнозата за 2023 г. е за приблизително 19 550 диагнози и 3 750 смъртни случая сред хора под 50-годишна възраст.
Колоректалният рак също така непропорционално засяга чернокожата общност в САЩ, където нивата са най-високи спрямо всички други расови/етнически групи. Афроамериканците са с около 20% по-голяма вероятност да развият колоректален рак и с около 40% по-голяма вероятност да умрат от него в сравнение с повечето други групи. Чернокожите американци често се сблъскват с по-сериозни препятствия пред превенцията, диагностицирането, лечението и преживяемостта при рак, включително системни расови неравенства, които са комплексни и надхвърлят очевидната връзка с онкологичните заболявания.
Обединено кралство
В Обединеното кралство около 41 000 души годишно се разболяват от рак на дебелото черво, което го прави четвъртият най-често срещан вид рак.
Австралия
Един на всеки 19 мъже и една на всеки 28 жени в Австралия ще развие колоректален рак преди 75-годишна възраст; един на всеки 10 мъже и една на всеки 15 жени ще го развият до 85-годишна възраст.
Папуа Нова Гвинея
В Папуа Нова Гвинея и други островни държави в Тихия океан, включително Соломоновите острови, колоректалният рак е много рядко срещан в сравнение с рак на белия дроб, стомаха, черния дроб или гърдата. Оценките сочат, че 8 на 100 000 души е вероятно да развият колоректален рак всяка година, докато 24 на 100 000 жени е вероятно да развият рак на гърдата.
Диагнозата колоректален рак при пациенти под 50-годишна възраст се нарича ранен колоректален рак (EOCC)
Случаите на EOCC са се увеличили през последното десетилетие особено сред популации на възраст между 20 и 40 години в Северна Америка Европа Австралия и Китай
Честота според възрастта
Честотата на колоректалния рак сред по-младите популации се е увеличила през последното десетилетие Въпреки че напредъкът в диагностичните процедури може да има известен ефект намалената вероятност за скрининг сред тези популации предполага че откривателският байъс не е основният фактор за тази тенденция По-вероятно е т нар ефекти на кохортата генерационни ефекти да са причина за нарастването
Най-голям ръст на случаите на EOCC се наблюдава сред мъже и жени на възраст 20–29 години като честотата се е увеличавала със 7.9% годишно в периода между 2004 и 2016 г По сходен начин макар и с по-ниска степен при мъже и жени на възраст 30–39 години се отчита нарастване от 3.4% годишно за същия период Въпреки това смъртността от колоректален рак остава непроменена
Рискови фактори
Рисковите фактори свързани с EOCC са подобни на тези при всички случаи на колоректален рак Наблюдаваните ефекти на кохортата най-вероятно са резултат от генерационни промени в начина на живот и околната среда
Превантивен скрининг
През 2018 г Американското дружество за борба с рака промени предишните си препоръки за скрининг на колоректален рак като понижи възрастта за започване на скрининга от 50 на 45 години след като беше установено увеличаване на случаите на EOCC Лица под 60-годишна възраст са идентифицирани като най-склонни да не участват в скринингови програми за колоректален рак